Presentación de caso
Recuperación de los tejidos perirradiculares en un paciente con tratamiento endodóntico
Recovery of periradicular tissues in a patient after endodontic treatment
Karina Lourdes Tito Moreno 1 * https://orcid.org/0009-0007-0705-1766
Pamela Mishell Cajo Yánez 1 https://orcid.org/0009-0007-3952-7108
Mathias Alejandro Navarrete Bustamante 1 https://orcid.org/0009-0004-4046-5029
1 Universidad de los Andes, UNIANDES, Ambato, Ecuador.
*Autor par la correspondencia. Correo electrónico: ualourdes91@uniandes.edu.ec
RESUMEN
La restauración de los tejidos perirradiculares después del tratamiento endodóntico es crucial para el éxito a largo plazo del tratamiento. Este estudio de caso tiene como objetivo presentar un paciente que recibió un tratamiento endodóntico en un molar con lesión periapical y la recuperación en los tejidos perirradiculares. Se observó una notable mejoría en la cicatrización y regeneración de los tejidos tras la terapia adecuada, que incluyó un seguimiento riguroso y el uso de técnicas de obturación y restauración adecuadas. La revisión bibliográfica enfatiza la importancia de un manejo adecuado de los tejidos perirradiculares para evitar complicaciones como infecciones recurrentes o la pérdida del diente tratado. Se concluye que la restauración exitosa de estos tejidos es clave para garantizar la durabilidad del tratamiento endodóntico.
Palabras clave: tejidos perirradiculares, tratamiento endodóntico, cicatrización, restauración, regeneración
ABSTRACT
The restoration of periradicular tissues following endodontic treatment is critical for the long-term success of the procedure. This case study presents the recovery of periradicular tissues in a patient who underwent endodontic treatment for a molar with periapical lesion. Significant improvement in healing and tissue regeneration was observed after appropriate therapy, which included strict follow-up and the use of proper obturation and restoration techniques. The literature review highlights the importance of proper management of periradicular tissues to avoid complications such as recurrent infections or loss of the treated tooth. It is concluded that successful restoration of these tissues is essential to ensure the durability of endodontic treatment.
Keywords: Periradicular tissues, endodontic treatment, healing, restoration, regeneration
Recibido: 16/06/2025.
Aprobado: 17/10/2025.
Editor: Yasnay Jorge Saínz.
Aprobado por: Silvio Emilio NIño Escofet.
Introducción
El tratamiento de conducto radicular o también llamado tratamiento de endodoncia es un procedimiento muy común en odontología, (1) el cual se desarrolla mediante un correcto diagnóstico, acceso a la cavidad pulpar, seguida de la instrumentación biomecánica y la obturación del sistema de conductos radiculares; todos estos pasos deben ser complementados por la irrigación y de ser necesario medicación intraconducto. (2) Este procedimiento se desarrolla de tal manera que se retira la pulpa infectada del diente y la cavidad de la raíz se desinfecta y se rellena con un material de sellado; (3) está indicado principalmente para pulpitis irreversible y la necrosis pulpar a causa de caries dental, incluso fisuras, fracturas o algún tipo de traumatismo. (1) Su finalidad es disminuir la mayor cantidad de carga bacteriana, (4) pero muchas de las veces los microorganismos causantes de la infección no son eliminados en su totalidad, por lo que luego de un periodo de tiempo desarrollan afecciones a nivel de la raíz como la lesión periapical. (3) La ausencia de dolor, inflamación y tracto sinuoso es un indicativo de éxito del tratamiento de conductos, (1) el cual a su vez basa también el éxito en la instrumentación adecuada, la desinfección integral y la obturación. (4)
Este procedimiento odontológico tiene como finalidad una desinfección del sistema de conductos radiculares lo más efectiva posible, ya que torna inviable el ambiente intraconducto para los microorganismos y de esta manera evitar el crecimiento y proliferación bacteriana con el uso de sustancias irrigadoras las cuales contienen propiedades antibacterianas que favorecen la reparación de los tejidos periapicales. (5) En los tejidos periapicales existen patologías para los cuales el tratamiento endodóntico está indicado, las que son la periodontitis apical sintomática y asintomática, así como también los abscesos periapicales agudos y crónicos, además de la osteítis condensante.(5)
La existencia de una lesión perirradicular es usualmente la consecuencia de una pulpa necrótica e infectada por la invasión de bacterias, sus toxinas y subproductos en el interior del sistema de conductos radiculares, lo cual provoca una respuesta inflamatoria que se produce como una reacción de defensa de los tejidos perirradiculares, estos son el periodonto y el hueso. Las reacciones que generalmente se evidencian son de tipo granulomatoso (granulomas perirradiculares). (6)
Las lesiones periapicales a su vez se clasifican según el daño periapical en 4 estadios: estadio 1, afección sin complicaciones ni problemas, de mínima gravedad, incluyen la ausencia o cambios mínimos en los tejidos periapicales; estadio 2, complicaciones limitadas al área periapical, riesgo significativamente mayor de complicaciones con respecto a la etapa 1. Hay un aumento en el tamaño de la lesión > 5 mm y la presencia de factores agravantes, como la complejidad del diente y la presencia de tracto sinuoso se presentan en esta categoría; estadio 3, pérdida ósea extensa más allá de la región apical inmediata con defectos óseos completos, radiolucideces grandes, defectos de furca e imágenes en forma de J; estadio 4, pérdida de dientes o desarrollo de complicaciones graves con pronóstico reservado. (5)
Las principales características de algunas de las patologías perirradiculares en las que se prefiere el tratamiento endodóntico es la visualización de imágenes radiolúcidas periapicales, estas se producen como consecuencia de la osteólisis que deriva de la acción de las bacterias y sus toxinas, las que pasan a través del conducto radicular hacia los tejidos periapicales. Esto se produce generalmente en una necrosis pulpar en donde se evidencia la respuesta inmune del organismo frente a la acción bacteriana, debido a que se “encapsulan” los procesos infecciosos, y generan las lesiones a nivel del periápice, a su vez se evidencian radiográficamente como imágenes radiolúcidas (5). La periodontitis apical es la implicancia de la infección endodóntica que se evidencia por la respuesta de defensa del huésped al estímulo microbial del sistema del conducto radicular, se conoce que es una lesión de carácter reversible, lo que quiere decir que sana espontáneamente luego del tratamiento. Puede ser de dos tipos, agudo o crónico, la de tipo agudo se manifiesta principalmente con dolor o abscesos; en el caso que un proceso agudo no se resuelve, evoluciona a un estado crónico. (7)
Las lesiones periapicales humanas son consideradas enfermedades infecciosas comunes que son inducidas por infecciones microbianas endodónticas, dado principalmente por microbios gramnegativos capaces de afectar el diente y el hueso alveolar circundante.(8) Los microorganismos existentes en el conducto radicular desempeñan un papel esencial en la iniciación y el establecimiento de lesiones perirradiculares, esta lesión de tipo asintomática alberga microorganismos anaerobios obligados. Así mismo, los microorganismos anaerobios grampositivos y facultativos predominan en las primeras etapas de la infección; (9) resaltando que la inflamación de los tejidos perirradiculares, se da inicio como una respuesta inmune o fisiológica del cuerpo ante la presencia de infección o contenido tóxico dentro del sistema de conductos radiculares, esta tiene como objetivo impedir el paso de bacterias al resto del organismo.
El paso de bacterias está en dependencia del grado de infección, si se sigue una clasificación se presenta del siguiente modo: grado I, conducto limpio; grado II, conducto no infeccioso; grado III, conducto infeccioso, y grado IV, conducto severamente infeccioso. En grados altos de infección se produce una respuesta inflamatoria que continua o a su vez deja secuelas como una lesión osteolítica donde radiográficamente, se observa como una sombra radiolúcida a nivel del periápice dental. (5) Las lesiones periapicales son consideradas una enfermedad osteolítica que ocurre en la región apical de la raíz. Presenta una prevalencia en la población adulta de alrededor del 6,3 % en todo el mundo; pero reducen la esperanza y la calidad de vida de los afectados. Su tasa de éxito en el tratamiento donde se incluye las realizadas por especialistas en endodoncia, es solo un poco más del 50 % después de 2 años de seguimiento. (8)
La remodelación ósea sucede cuando se altera la resorción y la formación ósea en orden cronológico. La resorción y la formación ósea son procesos opuestos y acoplados de osteoblastos y osteoclastos, que conjuntamente constituyen la masa ósea normal (10). Se entiende por lo tanto, que es un proceso complejo y dinámico que implica la interacción entre múltiples tipos de células, incluidos los osteoblastos, osteoclastos y células del sistema inmunológico. Las citoquinas juegan un papel crucial al mediar la comunicación entre estos sistemas, regulan la formación y resorción ósea mediante la modulación de la actividad celular. En la respuesta inmune inicial a una lesión ósea, los macrófagos y neutrófilos están encargados de la liberación de citoquinas y factores de crecimiento que son fundamentales para la curación. (11) Los osteoblastos son las células encargadas de formar hueso, se diferencian mediante factores de transcripción como runt y osterix, regulados por una red de citocinas. Algunas citocinas, como IL-10 e IFN-γ, promueven la osteoblastogénesis, mientras que otras, como TNF-α e IL-1α, la inhiben.(12)
Cuando un tejido es lesionado, el proceso de reparación se divide en tres etapas: inflamatoria, proliferativa y de remodelado. La fase inflamatoria, dura aproximadamente tres días, comienza con la hemostasia y la formación de un exudado tisular que atrae células proinflamatorias para eliminar toxinas y agentes irritantes, provoca vasodilatación, edema y acidosis local, lo cual contribuye al dolor. En la fase proliferativa, los fibroblastos migran al sitio lesionado, producen colágeno y favorecen la formación de nuevos vasos sanguíneos, al mismo tiempo genera tejido de granulación.
Finalmente, en la fase de remodelado, el tejido de granulación se convierte en cicatriz mediante la reestructuración de fibras de colágeno y la formación de una nueva red vascular. Asimismo, se inicia el proceso de osteogénesis y mineralización, que son fundamentales para restaurar completamente la función y estructura del tejido, especialmente en los tejidos óseos. Este proceso de reparación es continuo y dinámico, con solapamientos entre las fases. El tiempo del proceso de regeneración del hueso luego de un tratamiento de conductos varía en dependencia de varios factores, como el tipo de tratamiento, la gravedad de la lesión, la salud del paciente y el cuidado posoperatorio. En general el hueso alrededor de un diente tratado con endodoncia comienza a mostrar signos de curación dentro de los primeros 3 a 6 meses. (13) Sin embargo, la regeneración completa del hueso puede tardar entre 6 meses y 1 año, o incluso más en algunos casos. (14)
Para lograr un óptimo desarrollo de hueso, dos procesos son los encargados: modelado y remodelado óseo, el primero ocurre durante el crecimiento, produce cambios en tamaño y forma del hueso; el segundo se instaura durante toda la vida donde primero es reabsorbido por osteoclastos y formado en el mismo sitio por osteoblastos; forman la unidad metabólica básica que reconstruye el hueso de manera endocortical, intracortical y trabecular tanto de manera interna (endosteal) como externa (perióstica). (15)
Las dos células principales antes mencionados son provenientes de células mesenquimales y requieren activación del gen Osf2/Cbfa para su diferenciación. También de la utilización de citocinas, prostaglandinas y factores del crecimiento en su regulación; pero ciertos mediadores como IL-1, IL-6, TNF-𝛼, y TGF-𝛽 pueden contribuir a la reabsorción del hueso, debido a que las bacterias presentes en afecciones periodontales pueden estimular la producción de dichos mediadores inflamatorios y promueven la destrucción de los tejidos peridontales por acción de los mismos osteoclastos. Lo anterior se explica mediante los factores RANKL, RANK y OPG, ya que RANKL promueve la formación de osteoclastos al unirse con RANK, pero OPG evita dicha unión al existir bacterias que estimulen la producción de mediadores proinflamatorios, el factor RANKL se ve potenciado y juega un papel importante en la reabsorción ósea. (16)
La medicación intraconducto corresponde uno de los pasos fundamentales para el éxito de un tratamiento endodóntico puesto que no solo elimina microorganismos, también inactiva sus subproductos, el uso de esta permite al tanto al clínico como al paciente poder examinar si el pronóstico del tratamiento antes de la finalización de este. (17)
El hidróxido de calcio como medicamento intraconducto siempre ha sido la opción más utilizada a causa de su efectividad comprobada de desinfección de los canales radiculares durante los procesos endodónticos reparativos. Al mismo tiempo de reducir niveles de MMP-8 en los tejidos periapicales, debido a su expulsión de iones hidroxilos creando un ambiente con pH alto que inhibe microorganismos y neutraliza endotoxinas, ayuda a la mineralización, rompe materia orgánica y forma una barrera tanto física como química. Es recomendada en procedimientos que involucren procesos endodónticos reparativos. (18)
Dentro de las medicaciones de hidróxido de calcio, una de las más usades es UltraCal UX, que igualmente de presentar los beneficios del hidróxido de calcio convencional, este presenta más regulares y pequeñas partículas de HC, lo que mejora sus capacidades de humectación en la superficie dentinaria y favorece la penetración tubular. Así como también su acompañamiento con ultrasonido muestra resultados aún mayores en cuanto a penetración tubular. (19)
Otros beneficios del hidróxido de calcio no pueden ser examinados a simple vista, por ejemplo, este presenta reducción bacteriana de E. faecalis en un 86-96,5%. También actúa en la inflamación al reducir la expresión de TNF-α con el tiempo, conjuntamente promueve la liberación de TGF-β, favorece la reparación tisular lo cual conlleva a la proliferación y supervivencia de células madre, aunque se ha visto que este no reduce la expresión sobre la IL-10, puede contribuir al aumento de citocinas proinflamatorias. (20)
E. faecalis ha sido identificado como el agente bacteriano primario en casos de periodontitis apical debido a su resistencia y persistencia en los canales radiculares, así como su capacidad de desarrollar biolfim de una sola especie sin la necesidad de interactuar con demás microorganismos. En casos como este UltraCal UX ha demostrado efectividad aunado a sus beneficios antes mencionados, exhibe propiedades antibacterianas, desactiva lipopolisacáridos bacterianos y es bioinerte, aunque su efectivdad contra E.faecalis esté demostrada, medicamentos a base de HC reducen su potencial de acción contra bacterias facultativas específicas como Candida albican en conjunto con E. faecalis. (21)
Los cementos bioreactivos usados en los tratamientos endodónticos proveen un sellado del canal radicular, además de interacciones beneficiosas con los tejidos circundantes. Esto se debe a que el cemento es usado para rellenar los espacios entre la gutapercha y las paredes de dentina, mismo hecho que causa la mayoría de los fallos en el tratamiento puesto que a veces los espacios no son rellenados correctamente dando oportunidad a las bacterias que infiltren entre la dentina y el cemento. (22)
El cemento bioreactivo BioRoot RCS es un sellado de canales radiculares basado en silicato tricálcico, su interacción con los fluidos dentinarios puede conllevar a biomineralizacion; es decir, formación de minerales en el interior de los túbulos dentinarios mejoran su actividad biológica. (23)
El sistema de limas Reciproc Blue es un sistema reciprocante que posee una sección transversal en forma de S con tres tamaños de lima (R.25, R40 Y R50) y punta no cortante, con 08 de conicidad iniciada a tres milímetros de la punta de la lima. Dichas características permiten al sistema mantener un conducto centralizado, hacen que la tensión se reparta a lo largo del conducto y sus curvaturas, y dan un corte uniforme. (24,25) Su color característico es proveniente del tratamiento térmico aplicado en su fabricación, lo que le confiere además mayor flexibilidad, resistencia a la fatiga cíclica y menor marcas de microdureza superficial. (26,27)
Para llevar a cabo un tratamiento endodóntico completo se debe utilizar soluciones irrigantes, la más utilizada por los profesionales es el hipoclorito de sodio (NaOCl), por su actividad antimicrobiana ante un gran abanico de bacterias, hongos y virus, asimismo elimina patógenos que puedan desencadenar diferentes lesiones periapicales y fallos en los tratamientos; su capacidad disolvente de materia orgánica en glicerol y ácidos grasos disminuye la tensión superficial de la solución restante. (28,29) La concentración de 5,25 % de NaOCl ha sido documentada como la más efectiva en cuanto a desinfección y destrucción de microorganismos bacterianos. (30)
Como paso final de la desinfección, es recomendado el uso de solución EDTA, la cual permite la formación de quelatos de calcio y además de remover el smear layer de las paredes del conducto. (30) El objetivo de esta investigación consiste en objetivo presentar un paciente que recibió un tratamiento endodóntico en un molar con lesión periapical y la recuperación en los tejidos perirradiculares.
Método
El presente artículo consta de la presentación y reporte de un caso clínico provisto de un miembro docente de la carrera de Odontología de la facultad de Ciencias Médicas de la Universidad Regional Autónoma de los Andes “UNIANDES”, a la par que una revisión de la literatura actualizada. Las directrices del grupo CARE (CASE REPORTS) fueron tomadas como directrices para la realización del reporte de caso, mientras que la revisión de la literatura fue de tipo conceptual, de naturaleza cualitativa y carácter exploratorio, conformada de 32 artículos extraídos de bases de datos como PubMed, Elsevier, Google académico, SciELO, Cochrane y demás revistas con respaldo científico. Las referencias mínimas fueron 15, se escogieron artículos en idiomas como español e inglés. Los artículos fueron escogidos en base a los siguientes criterios de inclusión: remodelación ósea, lesión periapical, tratamiento de conducto radicular, hidróxido de calcio y así mismo fueron descartados en base a ciertos criterios de exclusión: resorción ósea, necrosis pulpar. Los resultados constituyen el diagnóstico y procedimientos realizados en cuanto al procedimiento endodóntico y posterior recuperación del órgano dentario, realizado por el profesional odontólogo facilitador del caso presente. Se usaron inteligencias artificiales como herramientas de búsqueda tales como ResearchRabbit y Consensus para agilizar la búsqueda de artículos e información utilizada.
Desarrollo
Paciente de 33 años acudió a un centro de salud público por presentar dolor y movilidad del órgano dentario # 12, donde le hicieron la apertura del conducto, pero se indicó que debido al grado de movilidad el órgano dentario debía ser extraído.
La paciente no aceptó este tratamiento por lo que buscó otra opinión, luego acude a la consulta privada en donde se le realizó la valoración clínica y radiográfica.
Clínicamente las pruebas de sensibilidad fueron negativas, a la percusión horizontal y vertical positivas y a la palpación también las pruebas fueron positivas, se apreció el órgano dentario un poco extruido en relación con los demás órganos dentarios de la arcada, además se observó la cavidad de la apertura inicial realizada y movilidad grado II del órgano dentario.
Radiográficamente se pudo observar una lesión radiolúcida de tamaño considerable a nivel apical, con pérdida ósea.
Se le explica a la paciente que puede realizarse el tratamiento endodóntico, pero que toca valorar la evolución de este con el tiempo, a través controles radiográficos y que después era probable que se debía colocar hueso y realizar cirugía apical en caso de que la lesión y movilidad no mejoraran. La paciente acepta el tratamiento y se procede a realizar el mismo.
Tratamiento
El OD # 12 fue diagnosticado con periodontitis apical sintomática, se realizó su preparación en un inicio de manera manual con la técnica coronoapical, comienza con una lima # 60 a nivel cervical y termina a nivel apical con una lima # 20, abundante irrigación con hipoclorito al 5,25 % y solución salina, se envió medicación intraconducto con UltraCal XS por 15 días. Transcurrido este tiempo la paciente no presenta sintomatología y se procede a retirar la medicación mediante irrigación y activación ultrasónica, se continúa con la instrumentación del conducto con la utilización del sistema mecanizado Reciproc Blue # 25, irrigación con hipoclorito en concentración del 5,25 %, activación ultrasónica y complementando en la irrigación final se usó EDTA al 17 %.
Para la obturación se utilizó la técnica de condensación lateral y se usó un cemento bioactivo BioRoot RCS.
Características radiográficas
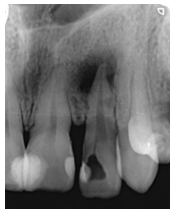
Figura 1: Radiografía inicial del órgano dentario 1.2 Se evidencia la apertura de la cavidad pulpar, afectación ósea y una lesión radiolúcida en el ápice. Fecha: 30/06/2022
Fuente: Dra. Karina Tito, 2022
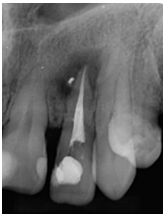
Figura 2: Radiografía final del órgano dentario 1.2 Tratamiento endodóntico finalizado y obturación completa. Fecha: 15/08/2022
Fuente: Dra. Karina Tito, 2022
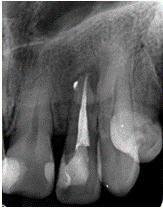
Figura 3: Control radiográfico después de 8 meses en donde se observa reparo óseo a nivel apical y recuperación de la cresta ósea. Fecha: 26/04/2023
Fuente: Dra. Karina Tito, 2023
Discusión
Mayorga. M & Cols mencionan que “el manejo del absceso periapical puede requerir cirugía periapical cuando las técnicas convencionales no son suficientes. En estos casos, la obturación simultánea con cirugía periapical y el uso de materiales de retro obturación ayudan a sellar el ápice y favorecen la regeneración ósea”. (7) Esta opción de tratamiento se considera efectiva cuando el tratamiento endodóntico convencional no es suficiente para resolver una infección o absceso periapical persistente. Este procedimiento implica en muchos casos la resección del ápice de la raíz, seguido de un sellado del extremo radicular, el proceso quirúrgico permite una recuperación ósea más rápida al eliminar de manera directa los focos de infección, lo cual favorece la regeneración ósea en el área afectada.
Por otro lado, Castillo. J y Alvares. M mencionan que “el éxito de un tratamiento endodóntico depende principalmente de la reparación de las lesiones periapicales, lo que se logra mediante un diagnóstico correcto, una preparación biomecánica correcta, además de una irrigación efectiva y un sellado apropiado del conducto radicular. En el caso de las lesiones periapicales, que incluyen quistes o granulomas, pueden curarse con un tratamiento bien realizado, en donde la eliminación de la carga bacteriana es clave para el éxito, ya que esta carga, que se encuentra principalmente en el biofilm del conducto, el cual debe reducirse mediante una adecuada irrigación”. (5)
De importancia a destacar es el potencial regenerativo de las células madre derivadas de la pulpa dental, se han estudiado ampliamente y dan como resultado que las células madre de la pulpa dental tienen propiedades comparables a las células madre de la medula ósea, (31) lo que provoca que en tratamientos en los que han utilizados células madre cultivadas y utilizadas por medio de un andamio de esponja a base de colágeno para defectos intraóseas periodontales, se obtuvieran mejores resultados en relación a regeneración periodontal; hecho que concuerda con afirmaciones hechas por Giulani. A & Cols que expresan resultados positivos de regeneración ósea y periodontal en pacientes con extracciones dentarias, que utilizan células madres de la pulpa junto con esponjas de colágeno, (32) así como, su potencial regenerativo se ha visto que no es afectado por el estado de inflamación de la pulpa misma aunque esta pierda, mínimamente capacidades osteogénicas y proliferativas, y mantenga funciones adipogénicas y condrogénicas, se recomienda el cultivo de estas células madres de pulpas inflamadas, apoyados en el argumento que podría tener efecto reparativo en tejidos duros afectados por periodontitis, (31) esto puede deberse a que el tejido óseo proveniente de células madre de la pulpa dental presenta mayor dureza debido a que estas no siguen las señales locales del hueso circundante, hecho que en si se puede considerar como un beneficio más a la hora de usar células madre como opción de tratamiento para la regeneración de tejidos perriradiculares. (32)
Conclusiones
El proceso de regeneración ósea tras una endodoncia es un proceso prolongado que depende críticamente de la eliminación total de los microorganismos del conducto radicular. Un tratamiento endodóntico efectivo, que incluya una desinfección meticulosa con instrumentos y materiales específicos, seguido de una obturación con cementos biorreactivos, es la base fundamental para prevenir infecciones y asegurar una cicatrización ósea exitosa.
Referencias
1. Mergoni G, Ganim M, Lodi G, Figini L, Gagliani M, Manfredi M. Single versus multiple visits for endodontic treatment of permanent teeth. Cochrane Database of Systematic Reviews .2022 [citado 19/03/2025];(12). Disponible en:
https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD005296.pub4/full
2. Pineda-Vélez E, Marín-Muñoz A, Escobar-Márquez A, Tamayo-Agudelo WF, Pineda-Vélez E, Marín-Muñoz A, et al. Factores relacionados con el resultado de los tratamientos endodónticos realizados en una institución universitaria con odontólogos en formación. CES Odontol. 2021 [citado 19/03/2025];34(1):14–24. Disponible en: http://www.scielo.org.co/scielo.php?script=sci_arttext&pid=S0120-971X2021000100014&lng=en&nrm=iso&tlng=es
3. Del Fabbro M, Corbella S, Sequeira-Byron P, Tsesis I, Rosen E, Lolato A, et al. Endodontic procedures for retreatment of periapical lesions. Cochrane Database of Systematic Reviews. 2016 [citado el 19/03/2025];2016(10). Disponible en: https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD005511.pub3/full
4. Khandelwal A, Janani K, Teja KV, Jose J, Battineni G, Riccitiello F, et al. Periapical Healing following Root Canal Treatment Using Different Endodontic Sealers: A Systematic Review. Biomed Res Int.2022 [citado el 19/03/2025];2022(1):3569281. Disponible en: https://onlinelibrary.wiley.com/doi/full/10.1155/2022/3569281
4. Castillo Páez JA, Álvarez M. Reparación de tejidos perirradiculares en el tratamiento endodóntico no quirúrgico. Una revisión. Rev.Científica Odontológica.2024 [citado 19/03/2025];12(3):e210. Disponible en:
https://pmc.ncbi.nlm.nih.gov/articles/PMC11495172/
5. Zmener O. Lesiones perirradiculares persistentes. Revisión narrativa. Rev Asoc Odontol Argent. 2022;1–12.
7. Mayorga-Solórzano MF, Naranjo-Yumi LF, Peñaherrera-Manosalvas MS. Regeneración de tejidos periradiculares mediante tratamiento endodóntico y cirugía paraendodóntica, regeneración ósea guiada (plasma rico en fibrina). Dominio de las Ciencias. 2017 [citado 19/03/2025];3(1):331–45. Disponible en: https://dominiodelasciencias.com/ojs/index.php/es/article/view/250/html
8. Song Y, Li X, Huang D, Song H. Macrophages in periapical lesions: Potential roles and future directions. Front Immunol .2022 [citado 19 /03/2025];13:949102. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC9483141/
9. Karamifar K, Tondari A, Saghiri MA. Endodontic Periapical Lesion: An Overview on the Etiology, Diagnosis and Current Treatment Modalities. Eur Endod J. 2020 [citado 19/03/2025];5(2):54. Disponible en:
https://pmc.ncbi.nlm.nih.gov/articles/PMC7398993/
10. Luo X, Wan Q, Cheng L, Xu R. Mechanisms of bone remodeling and therapeutic strategies in chronic apical periodontitis. Front Cell Infect Microbiol. 2022 [citado 19/03/2025];12:908859. Disponible en:
https://pmc.ncbi.nlm.nih.gov/articles/PMC9353524/
11. Yang N, Liu Y. The Role of the Immune Microenvironment in Bone Regeneration. Int J Med Sci. 2021 [citado 19/03/2025];18(16):3697. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC8579305/
12. Amarasekara DS, Kim S, Rho J. Regulation of Osteoblast Differentiation by Cytokine Networks. Int J Mol Sci. 2021 [citado el 19/03/2025];22(6):2851. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC7998677/
13. González A. Reparación apical posterior al tratamiento endodóntico - Apical repair after endodontic treatment. UNCuyo. 2016 [citado el 19/03/2025];1(1). Disponible en: https://bdigital.uncu.edu.ar/objetos_digitales/12128/gonzalez-rfoe-112016.pdf
14. Law A, Withrow J. Endodontic Case Difficulty Assessment and Referral. American Association of Endodontists. 2005 [citado19/03/2025]. Disponible en: https://www.aae.org/specialty/wp-content/uploads/sites/2/2017/07/ss05ecfe.pdf
15. Bilezikian J, Raisz L, Martin J. Principles of Bone Biology. 6ta. Ed. San Diego: Academic Press; 2008 [citado 19/03/2025].p.5–6. Disponible en:
16. Hienz SA, Paliwal S, Ivanovski S. Mechanisms of Bone Resorption in Periodontitis. J Immunol Res. 2015 [citado 19/03/2025];2015:615486. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC4433701/
17. Ordinola-Zapata R, Noblett WC, Perez-Ron A, Ye Z, Vera J. Present status and future directions of intracanal medicaments. Int Endod J.2022 [citado 19/03/2025];55(Suppl3):613. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC9321724/
18. Pekpinarli B, Kaval ME, Cogulu D, Ilhan B, Sorsa T, Tervahartiala T, et al. The effect of calcium hydroxide and double antibiotic paste on radiographic outcomes and periapical MMP-8 levels in regenerative endodontic procedures: a randomized clinical trial. Journal of Applied Oral Science. 2024 [citado 19/03/2025];32:e20240122. Disponible en: https://www.scielo.br/j/jaos/a/S7MBc8VDZFrVSqrqKLF7SjM/?lang=en
19. Peña-Bengoa F, Magasich MC, Bustamante D, Wastavino C, Niklander SE, Cáceres C. Effect of Ultrasonic Activation on Dentinal Tubule Penetration of Bio-C Temp and Ultracal XS: A Comparative CLSM Assessment. Eur Endod J. 2023 [citado 19/03/2025];8(4):268. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC10500209/
20. Binanzan N, Alsalleeh F. Cytokine Expression and Anti-Microbial Effectiveness of Different Calcium Hydroxide Dilutions. Indian Journal of Dental Research. 2022 [citado 19/03/2025];33(1):69–74. Disponible en:
https://journals.lww.com/ijdr/fulltext/2022/33010/cytokine_expression_and_anti_microbial.14.aspx
21. Patri G, Bansal S, Lath H, Chatterjee I, Majee N, Sinha Y. Comparative evaluation of the antibacterial efficacy of two experimental calcium silicate-based intracanal medicaments: An in-vitro study. Journal of Conservative Dentistry and Endodontics 2024 [citado 19/03/2025];27(4):419. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC11108418/
22. Bianco E, Calvelli C, Citterio CL, Pellegatta A, Venino PM, Maddalone M. Evaluation with micro-CT of the canal seal made with two different bioceramic cements: Guttaflow bioseal and bioroot RCS. Journal of Contemporary Dental Practice. 2020;21(4):359–66.
23. Kirthiga M, Thomas G, Jose S, Joseph S, Krishna M. Marginal Adaptation of BioRoot RCS, MTA-Fillapex, EpoxySeal, and Sealapex to Radicular Dentin: An In Vitro Study. Cureus. 2024 [citado 19/03/2025];16(7):e64380. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC11316956/
24. Ríos-Osorio N, Caviedes-Bucheli J, Murcia-Celedón J, Gutiérrez C, Sierra-Collazo D, Alvarado-Caicedo B, et al. Comparison of dynamic cyclic fatigue resistance of Reciproc® Blue and WaveOne® Gold after sterilization and/or immersion in sodium hypochlorite. J Clin Exp Dent .2024 [citado 19/03/2025];16(1):e1. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC10837797/
25. Nouroloyouni A, Shahi S, Milani AS, Noorolouny S, Farhang R, Azar AY. In vitro apical extrusion of debris and instrumentation time following root canal instrumentation with Reciproc and Reciproc Blue instruments and a novel stainless steel rotary system (Gentlefile) versus manual instrumentation. J Dent Res Dent Clin. 2023 [citado 19/03/2025];17(3):136. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC10676536/
26. Altufayli MD, Salim B, Katbeh I, Merei R, Mamasaidova Z. Shaping Ability of Reciproc Blue Versus One Curve in Curved Canal: An In-Vitro Study. Cureus. 2022 [citado 19/03/2025];14(4):e24387. Disponible en:
https://pmc.ncbi.nlm.nih.gov/articles/PMC9126444/
27. Al-labed H, layous K, Alzoubi H. The Efficacy of Three Rotary Systems (Reciproc Blue, WaveOne Gold, and AF Blue R3) in Preparing Simulated, Highly Curved Root Canals: An In Vitro Study. Cureus. 2022 [citado 19/03/2025];14(10):e30232. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC9650934/
28. Karkehabadi H, Khoshbin E, Abbasi R, Esmailnasab S, Doosti Irani A. Effects of Final Root Canal Irrigants in Conventional and Regenerative Endodontic Treatments: A Systematic Review. Avicenna Journal of Dental Research. 2024 [citado 19/03/2025];16(2):117–27. Disponible en: https://ajdr.umsha.ac.ir/Article/ajdr-1764
29. Mohammadi Z, Shalavi S, Kinoshita JI, Giardino L, Gutmann JL, Banihashem Rad SA, et al. A Review on Root Canal Irrigation Solutions in Endodontics. Journal of Dental Materials and Techniques. 2021 [citado 19/03/2025];10(3):121–32. Disponible en: https://jdmt.mums.ac.ir/article_18532.html
30. Dranceanu A, Andreea Diaconu O, Mihaela Gheorghiță L, Bătăiosu M, Dascălu I, Gabriela Nicola A, et al. Endodontic Irrigants: A Review. Dental Health Oral Res .2023 [citado 19/03/2025];4:1–8. Disponible en:
31. Alarcón-Apablaza J, Prieto R, Rojas M, Fuentes R. Potential of Oral Cavity Stem Cells for Bone Regeneration: A Scoping Review. Cells 2023 [citado 19/03/2025];12(10):1392. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC10216382/
32. Giuliani A, Manescu A, Langer M, Rustichelli F, Desiderio V, Paino F, et al. Three Years After Transplants in Human Mandibles, Histological and In-Line Holotomography Revealed That Stem Cells Regenerated a Compact Rather Than a Spongy Bone: Biological and Clinical Implications. Stem Cells Transl Med.2013 [citado 19/03/2025];2(4):316. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC3659838/
Declaración de conflicto de intereses
Los autores no declaran conflicto de intereses
Contribución de autoría
Los autores participaron en igual medida en la curación de datos, análisis formal, investigación, metodología, administración del proyecto, recursos, software, supervisión, validación, visualización, redacción – borrador original y redacción – revisión y edición.
![]() Los
artículos de la Revista
Correo Científico Médico perteneciente a la Universidad de Ciencias Médicas de
Holguín se comparten bajo los términos de la Licencia Creative Commons
Atribución 4.0 Internacional Email: publicaciones@infomed.sld.cu
Los
artículos de la Revista
Correo Científico Médico perteneciente a la Universidad de Ciencias Médicas de
Holguín se comparten bajo los términos de la Licencia Creative Commons
Atribución 4.0 Internacional Email: publicaciones@infomed.sld.cu