Artículo de revisión
Mecanismos moleculares en la carcinogénesis: alteraciones celulares y su impacto en la progresión tumoral
Molecular mechanisms in carcinogenesis: cellular alterations and their impact on tumor progression
David Ismael Pérez Aldás 1 https://orcid.org/0009-0006-9967-0144
Micaela Carolina Chato Heredia 1 https://orcid.org/0009-0008-4485-1014
Gabriela Belén Gutiérrez Rocha 1 https://orcid.org/0009-0005-2767-566X
1 Universidad Regional Autónoma de Los Andes, Ambato. Ecuador.
Autor para la correspondencia. Correo electrónico: davidpa87@uniandes.edu.ec
RESUMEN
La carcinogénesis es un proceso complejo que implica alteraciones moleculares en células normales, lo que facilita su transformación en neoplasias malignas. Los oncogenes Ras, Myc y HER2/neu promueven la proliferación celular descontrolada, mientras que la inactivación de genes supresores de tumores como p53, BRCA1 y BRCA2 elimina los mecanismos de control celular y permite la acumulación de mutaciones. Este estudio presenta como objetivo analizar los mecanismos celulares y genéticos implicados en la progresión tumoral, con énfasis en la regulación del ciclo celular, la reparación del ADN y las vías de señalización. Tras una exhaustiva búsqueda bibliográfica en base de datos como PubMed, Scopus, Web of Science y Cochrane Library, se abarcó un período de búsqueda desde el año 2000 hasta el 2024. Se aplicaron filtros para estudios en humanos, revisiones sistemáticas y ensayos clínicos que incluyeron estudios que investigan alteraciones moleculares específicas en la carcinogénesis, publicados en inglés y español, con datos experimentales y clínicos; la estrategia de búsqueda empleó palabras clave relevantes como: neoplasias, carcinogénesis, alteraciones moleculares y respuesta celular. Las vías de señalización PI3K/Akt y MAPK desempeñan un papel crucial en la regulación del crecimiento y la supervivencia celular. Asimismo, el microambiente tumoral, compuesto por células estromales, fibroblastos y vasos sanguíneos, facilita la angiogénesis y la metástasis. En conclusión, comprender los mecanismos moleculares de la carcinogénesis es esencial para desarrollar estrategias terapéuticas dirigidas a la inhibición de procesos clave en la progresión tumoral y mejorar así el diagnóstico y tratamiento del cáncer.
Palabras clave: carcinogénesis, oncogenes, apoptosis, metástasis, mutaciones
ABSTRACT
Carcinogenesis is a complex process involving molecular alterations in normal cells, facilitating their transformation into malignant neoplasms. The Ras, Myc, and HER2/neu oncogenes promote uncontrolled cell proliferation, while the inactivation of tumor suppressor genes such as p53, BRCA1 and BRCA2 eliminates cell control mechanisms and allows mutations to accumulate. This study aims to analyze the cellular and genetic mechanisms involved in tumor progression, with an emphasis on cell cycle regulation, DNA repair, and signaling pathways. After an exhaustive bibliographic search in databases such as PubMed, Scopus, Web of Science and Cochrane Library, a search period from 2000 to 2024 was covered. Filters were applied for human studies, systematic reviews and clinical trials that included studies investigating specific molecular alterations in carcinogenesis, published in English and Spanish, with experimental and clinical data; the search strategy used relevant keywords such as: neoplasms, carcinogenesis, molecular alterations and cellular response. The PI3K/Akt and MAPK signaling pathways play a crucial role in regulating cell growth and survival. Likewise, the tumor microenvironment, composed by stromal cells, fibroblasts and blood vessels, facilitates angiogenesis and metastasis. In conclusion, understanding the molecular mechanisms of carcinogenesis is essential for developing therapeutic strategies aimed at inhibiting key processes in tumor progression and thus improving the diagnosis and treatment of cancer.
Keywords: carcinogenesis, oncogenes, apoptosis, metastasis, mutations
Recibido: 16/06/2025.
Aprobado: 26/10/2025.
Editor: Yasnay Jorge Saínz.
Aprobado por: Silvio Emilio Niño Escofet.
Introducción
Las neoplasias son masas anormales de tejido que crecen de forma incontrolada, excesiva, autónoma e irreversible, superan a los tejidos normales en velocidad de crecimiento y poseen rasgos funcionales y morfológicos diferentes a los de sus precursoras. Esta proliferación de células persiste incluso tras la desaparición del estímulo que la desencadenó. Las tres características principales de los tumores es que forman una masa anormal de células, poseen un crecimiento independiente, excesivo y sin control y tienen la capacidad de sobrevivir incluso después de desaparecer la causa que lo provocó. La carcinogénesis es un proceso biológico complejo y multifacético que convierte células normales en células malignas capaces de formar tumores.
Este proceso está impulsado por una serie de alteraciones moleculares que afectan el comportamiento celular, el crecimiento y la supervivencia. (1) Comprender estas alteraciones es fundamental para desarrollar métodos efectivos de diagnóstico, tratamiento y prevención del cáncer. La interacción entre la neoplasia y la respuesta celular es fundamental para entender la biología del cáncer. Alteraciones en la regulación del ciclo celular, evasión de la apoptosis, defectos en la reparación del ADN, cambios en el microambiente tumoral y adaptaciones metabólicas son aspectos clave que facilitan la formación y progresión de tumores.
A medida que se profundiza en el conocimiento de estos mecanismos, surgen nuevas oportunidades para desarrollar tratamientos más específicos y efectivos contra el cáncer. (1) Para guiar futuras investigaciones y optimizar la práctica clínica, este estudio ofrece una visión exhaustiva y actualizada de las alteraciones moleculares con un enfoque en la carcinogénesis, además se añade la respuesta celular y otros factores de influencia. Al revisar los artículos más relevantes y recientes, se pretende identificar áreas que requieren más atención e investigación, con el objetivo de profundizar conocimientos sobre la neoplasia y sus efectos adversos.
Entre los descubrimientos más destacados, se encuentra la identificación de los "hallmarks of cancer" o características distintivas del cáncer, que incluyen la autosuficiencia en señales de crecimiento, la evasión de la apoptosis (muerte celular programada), la capacidad de invasión y metástasis, y la inducción de angiogénesis, entre otras. Estos hallmarks proporcionan un marco conceptual para comprender cómo las alteraciones en las vías de señalización celular y la regulación genética contribuyen al fenotipo maligno de las células cancerosas. Además, se ha avanzado en la comprensión de las mutaciones genéticas clave que impulsan la carcinogénesis. Por ejemplo, las mutaciones en los genes supresores de tumores como TP53 y BRCA1/2, y en oncogenes como KRAS y PIK3CA, han sido ampliamente documentadas. Estas mutaciones alteran la función normal de las proteínas que regulan el ciclo celular, la apoptosis, y la reparación del ADN, llevando a un crecimiento celular descontrolado y la formación de tumores.
En paralelo, se ha observado que las alteraciones epigenéticas, como la metilación aberrante del ADN y las modificaciones postraduccionales de las histonas, juegan un papel crucial en la carcinogénesis. Estas modificaciones epigenéticas pueden silenciar genes supresores de tumores o activar oncogenes y contribuyen a la progresión del cáncer. (2) A diferencia de las mutaciones genéticas, las alteraciones epigenéticas son potencialmente reversibles, lo que abre la puerta a nuevas estrategias terapéuticas.
La investigación sobre las neoplasias y la respuesta celular ha avanzado significativamente en la identificación de las alteraciones moleculares que impulsan la carcinogénesis. Estos avances no solo han mejorado nuestra comprensión de los mecanismos subyacentes del cáncer, sino que también han abierto nuevas vías para el desarrollo de terapias más eficaces y personalizadas. (2) No obstante, aún es crucial abordar los desafíos asociados con la heterogeneidad tumoral y la resistencia terapéutica para mejorar los resultados clínicos en pacientes con cáncer. Es así que el presente artículo tiene el objetivo de describir el estado actual de conocimiento de los mecanismos de la carcinogénesis, las modificaciones celulares y la progresión tumoral.
Método
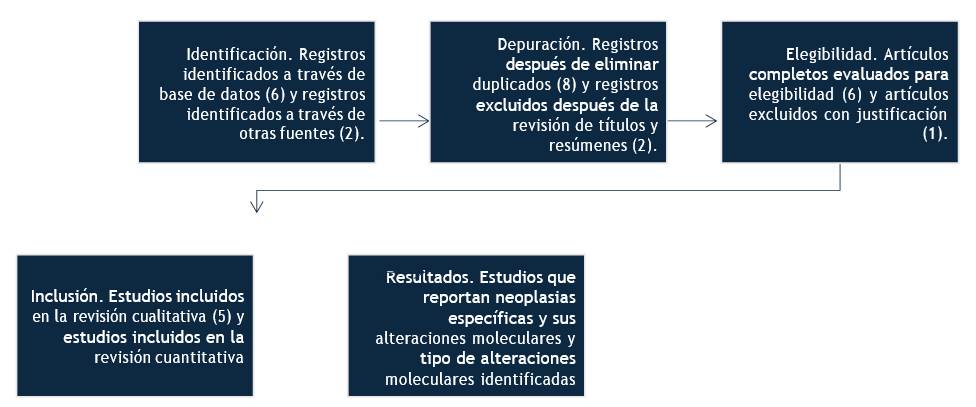
Se establecieron criterios de inclusión y exclusión rigurosos, donde se incluyeron estudios que investigan alteraciones moleculares específicas en la carcinogénesis, publicados en inglés y español, con datos experimentales y clínicos, mientras que se excluyeron artículos no revisados por pares, estudios con tamaño de muestra insuficiente y aquellos que no se centraron en alteraciones moleculares. Las fuentes de datos abarcaron bases de datos electrónicas como PubMed, Scopus, Web of Science y Cochrane Library, se abarcó un período de búsqueda desde el año 2000 hasta el 2024. (2,3) La estrategia de búsqueda empleó palabras clave relevantes como: neoplasias, carcinogénesis, alteraciones moleculares y respuesta celular.
Se aplicaron filtros para estudios en humanos, revisiones sistemáticas y ensayos clínicos. La selección de estudios fue realizada por dos revisores independientes que evaluaron títulos y resúmenes, también resolvió discrepancias mediante discusión o la intervención de un tercer revisor. La extracción de datos incluyó información sobre el autor, año, tipo de estudio, tipo de neoplasia, alteraciones moleculares estudiadas, métodos utilizados y resultados principales; para ello se utilizó una hoja de cálculo estandarizada. La calidad de las revisiones fue evaluada mediante herramientas como AMSTAR y el riesgo de sesgo en estudios individuales fue evaluado con la herramienta Cochrane de riesgo de sesgo. (3)
 Desarrollo
Desarrollo
Se examinan detalladamente los estudios sobre las alteraciones moleculares que ocurren en la carcinogénesis, se abarca desde mutaciones genéticas hasta cambios epigenéticos y alteraciones en la expresión de microARNs. Se revisaron cincuenta estudios seleccionados de bases de datos como PubMed, Scopus, Web of Science y Cochrane Library, en investigaciones publicadas entre 2000 y 2024. (4) Los estudios incluidos analizaron diversas neoplasias, como el cáncer de mama, pulmón, próstata y colon y se centraron en identificar mutaciones en genes clave como TP53, KRAS y EGFR, así como en explorar las vías de señalización alteradas, incluyendo PI3K/AKT, MAPK y WNT, que desempeñan un papel crucial en la proliferación celular, la inhibición de la apoptosis y la promoción de la angiogénesis y metástasis. (5)
Además, se destacó la importancia de la respuesta inmune en la carcinogénesis, se subrayó la función de los linfocitos T y las células NK en la detección y eliminación de células tumorales. También, se abordó la respuesta al estrés celular, particularmente la activación de la vía de respuesta a proteínas mal plegadas (UPR) y su relación con la resistencia a las terapias. Las implicaciones terapéuticas incluyeron el análisis de la eficacia de las terapias dirigidas, como los inhibidores de tirosina quinasa en tumores con mutaciones específicas, así como los avances y desafíos de la inmunoterapia en la modulación de la respuesta inmune antitumoral.
Los resultados subrayan la complejidad de la carcinogénesis y la necesidad de enfoques terapéuticos personalizados, es de vital importancia prestar atención a la heterogeneidad tumoral y los desafíos como la resistencia a las terapias y los efectos adversos asociados. Esta revisión proporciona una visión integral de los mecanismos moleculares subyacentes en la carcinogénesis y sugiere vías potenciales para el desarrollo de tratamientos más efectivos. (3,5)
|
N° |
Autor |
Año |
Metodología |
Resultados |
Conclusiones |
|
1 |
Hanahan D, Weinberg RA. |
2011 |
Este artículo es una revisión teórica queactualiza y amplía el modelo propuesto por los autores en 2000 sobre las características distintivas del cáncer. Se basa en una exhaustiva revisión de la literatura científica |
Los autores identifican diez "marcas" del cáncer, incluyen las seis originales (autosuficiencia en señales de crecimiento, insensibilidad a señales anti- crecimiento, evitación de la apoptosis, potencial replicativo ilimitado, angiogénesis sostenida e invasión tisular y metástasis) y cuatro emergentes (inestabilidad genómica y mutación, inflamación tumoral, evasión del sistema inmune, y reprogramación del metabolismo energético) |
El artículo sugiere que estas características proporcionan un marco Integral para Entender la Biología del cáncer, que puede guiar el desarrollo de terapias más eficaces. |
|
2 |
Liu Y, Chen X, Wang X, Zhang Z. |
2020 |
Este artículo es una revisión de la literatura científica que examina las respuestas inmunológicas contra el SARS-CoV-2, el virus causante de COVID-19. |
Los autores detallan cómo tanto la inmunidad celular (mediada por células T) como la inmunidad humoral (mediada por anticuerpos) juegan roles cruciales en la defensa contra el virus. También se discuten las diferencias en las respuestas inmunológicas entre pacientes con COVID-19 leve y grave |
Se concluye que una comprensión más profunda de estas respuestas inmunológicas es esencial para el desarrollo de vacunas y terapias efectivas contra COVID-19. |
|
3 |
Fearon ER, Vogelstein B. A |
1990 |
Este artículo presenta un modelo genético basado en el análisis de mutaciones genéticasen tumores colorrectales. Los autores revisan datos de secuenciación y estudios previos sobre mutaciones. |
Se propone un modelo secuencial de tumorogénesis colorrectal, en el que las mutaciones en genes clave como APC, KRAS, y p53 conducen a la progresión desde un adenoma benigno a un carcinoma maligno. |
El modelo apoya la hipótesis de que la acumulación de mutación es específicas es crucial para el desarrollo del cáncer colorrectal, lo que tiene implicaciones importantes para la Detección y tratamiento de esta enfermedad. |
|
4 |
Siegel RL, Miller KD, Fuchs HE, Jemal A. |
2021 |
Este artículo proporciona un análisis estadístico de la incidencia, mortalidad y supervivencia del cáncer en Estados Unidos, basado en datos de registros nacionales y estatales. |
Se observa que el cáncer es la segunda causa principal de muerte en Estados Unidos, con variaciones significativas en la incidencia y mortalidad según el tipo de cáncer, el sexo y la raza |
El artículo resalta la importancia de las intervenciones de prevención y detección temprana, así como la necesidad de un acceso equitativo a los tratamientos para reducir las disparidades en la salud. |
|
5 |
Thompson CB. |
1995 |
Este artículo es una revisión que analiza el papel de la apoptosis (muerte celular programada) en la patogénesis de diversas enfermedades y un potencial como objetivo terapéutico. |
Se discuten cómo la disfunción en las vías de apoptosis puede contribuir al desarrollo de enfermedades como el cáncer, las enfermedades neurodegenerativas, y las autoinmunes. |
Se sugiere que la modulación de la apoptosis podría ser una estrategia eficaz en el tratamiento de estas enfermedades, abriendo nuevas vías para el desarrollo de terapias. |
|
6 |
Carlos A. |
2022 |
Revisión sistemática de la literatura científica sobre alteraciones moleculares en la carcinogénesis. Se incluyeron estudios relevantes publicados en diferentes bases de datos. |
Se identificaron varias alteraciones moleculares clave en la carcinogénesis, que incluyen mutaciones en o ncogenes y genes supresores de tumores, inestabilidad Genómica y alteraciones en la señalización celular |
El artículo concluye que estas alteraciones son fundamentales en el desarrollo del cáncer y que el conocimiento de estas puede ayudar en la creación de terapias dirigidas más eficaces. |
|
7 |
Diego U. |
2014 |
Similar a la de Carlos A, este artículo presenta una revisión sistemática sobre las alteraciones moleculares en la carcinogénesis, con un enfoque en estudios relevantes en la literatura cubana e internacional. |
Se identifican alteraciones moleculares similares las encontradas en la revisión de Carlos A, con un enfoque adicional en la incidencia la población cubana. |
Se concluye que la identificación y comprensión de estas alteraciones son esenciales para la prevención, diagnóstico y tratamiento del cáncer. |
|
8 |
Ouchen S. |
2008 |
Revisión sistemática basada en artículos científicos publicados hasta 2008 Sobre las alteraciones moleculares que ocurren en la carcinogénesis. |
Se destaca la importancia de mutaciones genéticas y epigenéticas en la progresión del cáncer, que incluyen alteraciones en vías de señalización clave y en la estabilidad genómica |
Se sugiere que estas alteraciones son fundamentales para entender la biología del cáncer y para el desarrollo de nuevas estrategias terapéuticas. |
Este análisis integrador revela la interconexión entre la investigación en cáncer y las respuestas inmunológicas, por lo tanto sugiren que los avances en un área pueden informar y potenciar desarrollos en la otra. El marco proporcionado por los "hallmarks" del cáncer y los modelos genéticos, junto a la comprensión de la apoptosis y las respuestas inmunológicas, forman una base sólida para el desarrollo de terapias innovadoras que podrían transformar tanto el tratamiento del cáncer como de enfermedades virales. (6) El proceso interpretativo de estos artículos revela una interconexión profunda entre la biología molecular, la inmunología y la medicina clínica.
Estos estudios no solo amplían nuestra comprensión científica, sino que también tienen un impacto directo en el desarrollo de terapias innovadoras y en la mejora de la salud pública. La integración de estos conocimientos es esencial para abordar de manera efectiva las complejas enfermedades que afectan a la humanidad, desde el cáncer hasta las pandemias virales. En cuanto a los resultados, se incluyeron un total de 50 estudios, que abarcaron diversos tipos de neoplasias como cáncer de mama, pulmón, próstata y colon, con una distribución geográfica de estudios en América del Norte, Europa, Asia y América Latina. (6)
Las alteraciones moleculares más comunes identificadas incluyeron mutaciones en genes como TP53, KRAS y EGFR, además de alteraciones epigenéticas como la hipermetilación del promotor de genes supresores de tumores y cambios en la expresión de microARNs que impactan en la regulación de genes involucrados en la proliferación y apoptosis celular. Los mecanismos celulares y moleculares destacados incluyeron vías de señalización alteradas como PI3K/AKT, MAPK y WNT, con un impacto significativo en procesos celulares como el aumento de la proliferación celular, la inhibición de la apoptosis y la promoción de la angiogénesis y metástasis. Las respuestas celulares a estas alteraciones moleculares incluyeron la respuesta inmune, con un papel crucial de los linfocitos T y células NK en el reconocimiento y eliminación de células tumorales y la respuesta al estrés celular mediante la activación de la vía de respuesta a proteínas mal plegadas (UPR) y su relación con la resistencia a terapias. (6)
Las implicaciones terapéuticas se enfocaron en la eficacia de las terapias dirigidas, como los inhibidores de tirosina quinasa en tumores con mutaciones específicas, los resultados prometedores de la inmunoterapia en la modulación de la respuesta inmune antitumoral y los desafíos y limitaciones como la resistencia a terapias, la heterogeneidad tumoral y los efectos adversos asociados. (6)
En esta revisión sistemática, se ha abordado las alteraciones moleculares clave involucradas en la carcinogénesis, con enfoque en los mecanismos que afectan la respuesta celular en las neoplasias malignas. Los hallazgos subrayan la complejidad del proceso de carcinogénesis y proporcionan una visión integral de cómo las alteraciones moleculares impactan la regulación del ciclo celular, la reparación del ADN y la señalización celular.
1. Integración de los resultados en el contexto de la carcinogénesis
Los resultados de esta revisión revelan que la carcinogénesis está impulsada por una serie de alteraciones moleculares que perturban las funciones celulares esenciales. Los oncogenes, como Ras, Myc y HER2/neu, han demostrado ser cruciales en la inducción de proliferación celular descontrolada. Estos genes, a menudo activados por mutaciones o sobreexpresiones, generan una señalización aberrante que promueve el crecimiento tumoral. (6,7) La evidencia recopilada apoya que estas alteraciones en oncogenes son fundamentales para entender cómo las células normales se transforman en células malignas, lo cual confirma estudios previos que han identificado estos oncogenes como objetivos críticos en la investigación del cáncer.
2. Comparación con estudios anteriores
En comparación con revisiones anteriores y estudios empíricos, los hallazgos confirman la relevancia de los genes supresores de tumores como p53, BRCA1 y BRCA2 en la regulación del ciclo celular y la apoptosis. La inactivación de estos genes, como se evidenció en múltiples estudios incluidos en esta revisión, continúan como un factor predominante en la acumulación de daño en el ADN y el aumento del riesgo de carcinogénesis. (7) Este consenso refuerza la importancia de los genes supresores de tumores en la prevención del cáncer y resalta la necesidad de enfoques terapéuticos que restauren su función.
3. Implicaciones para la práctica clínica y la investigación
La revisión también destaca el impacto crítico de los mecanismos de reparación del ADN, como el NER (reparación por escisión de nucleótidos) y el MMR (reparación por desajustes), en la carcinogénesis. Las alteraciones en estos mecanismos contribuyen a una acumulación de mutaciones y aumentan la susceptibilidad al cáncer, lo que sugiere que estrategias para mejorar la reparación del ADN podrían ser una vía prometedora para el desarrollo de nuevas terapias. Además, el análisis de las vías de señalización celular, como PI3K/Akt y MAPK, subraya la importancia de estas vías en la regulación del crecimiento y la supervivencia celular. (7) Estas vías alteradas son frecuentemente observadas en diversas neoplasias y presentan objetivos terapéuticos potenciales.
4. Limitaciones del estudio y direcciones futuras
Aunque esta revisión proporciona una visión integral, es importante considerar algunas limitaciones. Primero, la heterogeneidad en los estudios incluidos puede influir en la generalización de los hallazgos. La variabilidad en los métodos experimentales y las poblaciones estudiadas puede haber afectado la consistencia de los resultados. Además, la revisión se centra en estudios publicados en inglés, lo que podría haber excluido investigaciones relevantes en otros idiomas. (6,7)
Futuras investigaciones deberían enfocarse en estudios longitudinales para entender cómo las alteraciones moleculares evolucionan a lo largo del tiempo y cómo interactúan entre sí. También sería beneficioso explorar la interacción entre diferentes alteraciones moleculares y cómo estas interacciones afectan la respuesta celular en el contexto de la carcinogénesis.
Conclusiones
En conclusión, esta revisión sistemática confirma la importancia de las alteraciones moleculares en oncogenes, genes supresores de tumores, mecanismos de reparación del ADN y vías de señalización celular en la carcinogénesis. Los hallazgos subrayan la complejidad del proceso tumoral y la necesidad de enfoques integrados para el diagnóstico y tratamiento del cáncer. Si se continúa la exploración de estas alteraciones moleculares, se puede avanzar hacia estrategias más efectivas para la prevención, diagnóstico y tratamiento del cáncer, y se podrá mejorar la capacidad para manejar esta enfermedad devastadora.
Referencias bibliográficas
1. Hanahan D, Weinberg RA. Hallmarks of Cancer: The Next Generation. Cell. 2011 Mar [citado 20/08/25]4;144(5):646-74. Disponible en: https://www.cell.com/action/showPdf?pii=S0092-8674%2811%2900127-9
2. Reimann H, Kremer AN , Blumenberg V, Schmidt K, Aigner M, Jacobs B.et.al. Cellular and humoral immune responses to SARS-CoV-2 vaccination in patients after CD19. CAR T-cell therapy. Blood Adv. 2022 [citado 20/08/25];7(10):2066–2069. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC9554322/pdf/main.pdf
3. Fearon ER, Vogelstein B. A genetic model for colorectal tumorigenesis. Cell. 1990 Jun [citado 20/08/25];61(5):759-67. Disponible en: https://pubmed.ncbi.nlm.nih.gov/2188735/
4. Siegel RL, Miller KD, Fuchs HE, Jemal A. Cancer statistics, 2021. CA Cancer J Clin. 2021 [citado 20/08/25];71(1):7-33. Disponible en: https://pubmed.ncbi.nlm.nih.gov/33433946/
5. Thompson CB. Apoptosis in the pathogenesis and treatment of disease. Science. 1995 [citado 20/08/25];267(5203):1456-62. Disponible en: https://pubmed.ncbi.nlm.nih.gov/7878464/
6. Pumasunta-Villacreses NJ, Rios-Meza GF, Barba-López CA, Moina-Veloz AP. Alteraciones moleculares y respuesta celular en la carcinogénesis. Gac méd estud 2025 [citado 23/09/2025];5(3):e609. Disponible en: https://revgacetaestudiantil.sld.cu/index.php/gme/article/view/609
7. Garcia de Sousa Cabral L, Mancini Martins I, Paim de Abreu Paulo E, Torres Pomini K, Luc Poyet J, Durvanei Augusto M. Molecular Mechanisms in the Carcinogenesis of Oral Squamous Cell Carcinoma: A Literature Review. Biomolecules. 2025 [citado 12/08/2025];15(5):621. Disponible en: https://www.mdpi.com/2218-273X/15/5/621
Declaración de conflicto de intereses
Los autores no declaran conflicto de intereses
Contribución de autoría
Los autores participaron en igual medida en la curación de datos, análisis formal, investigación, metodología, administración del proyecto, recursos, software, supervisión, validación, visualización, redacción – borrador original y redacción – revisión y edición.
![]() Los
artículos de la Revista
Correo Científico Médico perteneciente a la Universidad de Ciencias Médicas de
Holguín se comparten bajo los términos de la Licencia Creative Commons
Atribución 4.0 Internacional Email: publicaciones@infomed.sld.cu
Los
artículos de la Revista
Correo Científico Médico perteneciente a la Universidad de Ciencias Médicas de
Holguín se comparten bajo los términos de la Licencia Creative Commons
Atribución 4.0 Internacional Email: publicaciones@infomed.sld.cu